زئولیت چیست؟
دستهای از مواد متخلخل معروف به زئولیتها هستند که معمولا حفرههایی کوچکتر (nm2>) از آئروژلها یا سیلیکون متخلخل دارند. زئولیتها نه فقط حفراتی با اندازهی یکنواخت دارند؛ بلکه به صورت تناوبی آرایش مییابند تا نظم دور برد داشته باشند. این مواد بلورین هستند. برخی از زئولیت به صورت طبیعی وجود دارند. با این وجود، به علت اهمیت صنعتی آنها به عنوان کاتالیزور و مواد بسیار جاذب، آنها در مقیاس زیاد نیز سنتز میشوند.
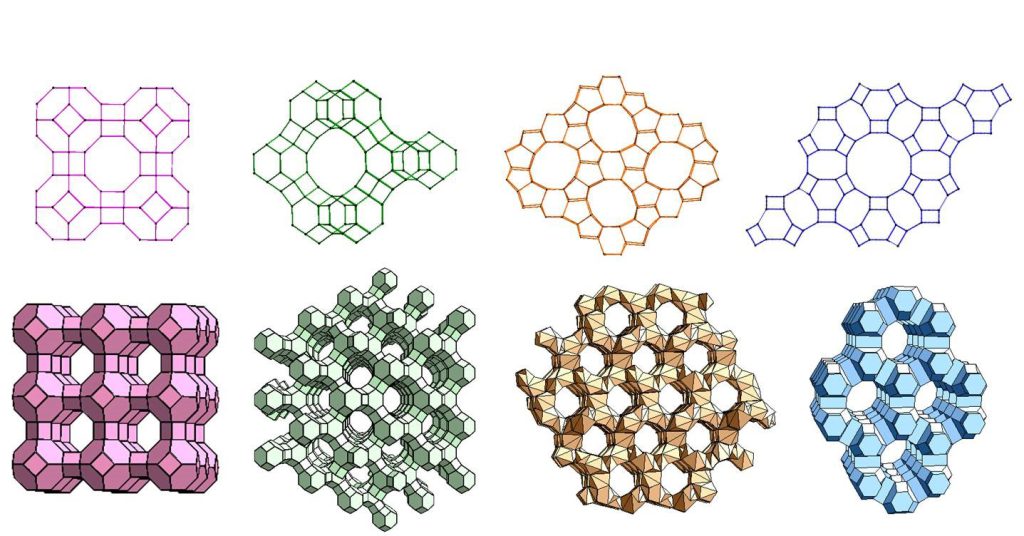
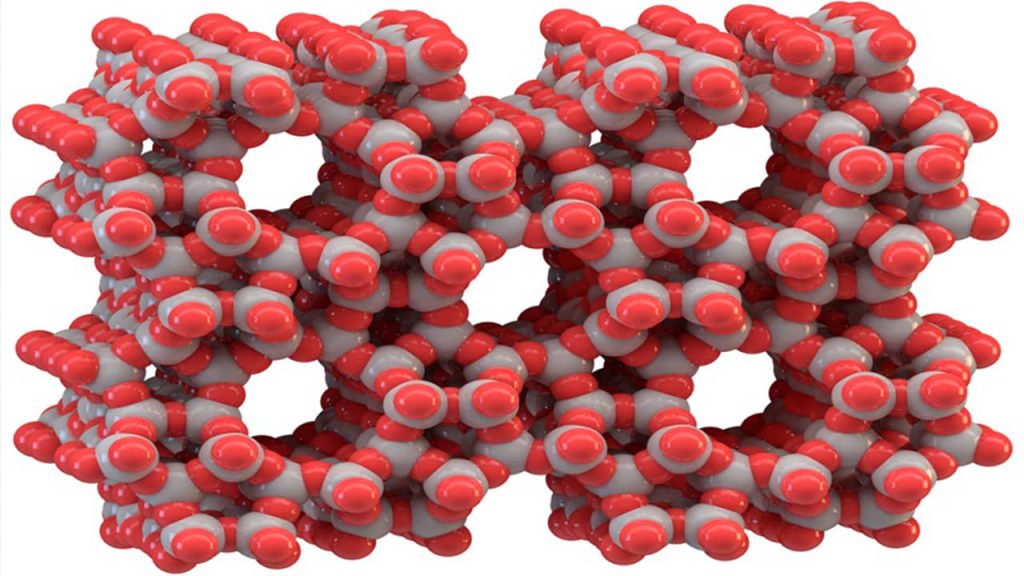
کلمهی زئولیت از دو واژهی “زئو” و “لیتوس” که به ترتیب به معنای “جوشیدن” و “سنگ” هستند، نشات می گیرد و به این صورت است که بیرون جوشیدن آب از برخی مواد، آنها را به زئولیتهای متخلخل تبدیل میکند. آنها ساختارهای بلورینی با نظم دور برد برای هر یک از سلولهای واحدشان در سه بعد دارند. سلول واحد خودش غالبا نتیجهای از برخی زیرواحدهای کاملا پیچیده است. متداولترین زئولیتها همراه با واحدهای سازندهای از واحدهای چهاروجهی از (Si) و (Al) هستند که توسط پیوندهایی از نوع Si-O-Al به هم متصل هستند. پیوندهای Si-O-Si نیز میتوانند در زئولیتها وجود داشته باشند ولی هیچ پیوند Al-O-Al وجود ندارد. این نشان میدهد که همیشه تعداد اتمهای سیلیکون با Al برابر یا بیشتر است.
ظرفیت سیلیکون 4 و ظرفیت آلومینیوم 3 است. این به این معناست که با جایگزینی Al، بار منفی اضافی روی شبکه وجود دارد که نیاز است متعادل گردد. این کار با افزایش چند کاتیون یا پذیرندههای الکترونی در این مواد انجام میشود. پس یک فرمول عمومی برای زئولیت را میتوان به صورت زیر نوشت:
Z H2O [ Alx SiyO2(x+y) ]Mx
این ماده به آلومینوسیلیکات نیز معروف است. علاوه بر این برخی واحدهای چهاروجهی دیگر مانند (GeO4)، (ZnO4)، (PO4) و … نیز میتوانند وجود داشته باشند که به جای Al یا همراه آن به کار روند. در حدود 40 زئولیت طبیعی وجود دارد و تعداد خیلی بیشتری را نیز میتوان سنتز کرد.
سنتز زئولیتها
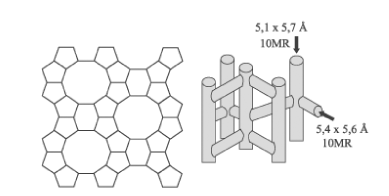
سنتز زئولیتها کاملا تعادلی بین مواد افزودنی و شرایط فرایند است. اغلب افزودنیهای آلی آمونیومی یا آمینها باید با مقادیر مناسبی افزوده شوند. عقیده بر این است که کاتیونهای فلزی و افزودنیهای آلی هر دو به عنوان قالبهایی برای ساختن ساختارهای مختلف عمل میکنند. تغییر Si/Al؛ Si/H2O؛ Si/کاتیون و افزودنیهای آلی میتواند زئولیتهای زیادی را بیشتر از تعداد زئولیتهای طبیعی تولید کند. برخی از گونههای شیمیایی، مسئول دستیابی به ساختار ویژهای در زئولیتها هستند. چنین گونههای شیمیایی نقش قالبهای مولکولی معروف را ایفا میکنند. با این وجود با استفاده از بیش از یک مولکول آلی، ساختار ویژهای را میتوان به دست آورد و یک مولکول میتواند ساختارهای مختلفی را برای پیشروهای مختلف که زئولیتها را تشکیل میدهند، ایجاد کند. محلولهای سیلیکا و آلومینیوم پیشرو هیدرولیز شده و مانند فرایند سل – ژل، چند تراکمی روی میدهد. واکنشگرهای آلی و معدنی اضافه شده و ژلی که به ترتیب تشکیل میگردد، در یک اتوکلاو در فشار (چند ده میلیبار) و دمای بالا (معمولا 100 تا 350 درجهی سلسیوس) هیدرولیز میشوند. قطر حفرات را میتوان با توزیع اندازهی باریکی در محدودهی اندازهی 3.0 تا 0.2 نانومتر کنترل کرد. حفرات میتوانند به صورت D-1، D-2 یا D-3 به هم متصل شوند. چنین مواد متخلخلی کاربردهای زیادی پیدا میکنند. در تصویر شمارهی 1، ساختار یک زئولیت ZSM-5 که بسیار پرکاربرد است نشان داده میشود.
خواص زئولیتها
- زئولیتها موادی بلورین و شدیدا متخلخل منظم هستند.
- اندازهی حفرات را میتوان دقیقا کنترل کرد.
- زیر واحدهای زیادی میتوانند وجود داشته باشند که زئولیتها با واحدهای سازندهی مختلف را تشکیل میدهند.
- حفرات در زئولیتها برای انجام واکنشهای مختلف مفیدند.
- زئولیتها، کاتالیزورها یا مواد جاذب مفیدی هستند.
- با کنترل اندازهی حفرات تا مقدار دلخواه، سنتز و سازماندهی نانو ذرات درون زئولیتها امکانپذیر است.